Faciliter la gestion des (re) qualifications équipements et le maintien en état validé grâce à la digitalisation
Dans les industries réglementées telles que les lifesciences, chaque équipement doit faire l’objet d’un processus de qualification documenté pour garantir la conformité réglementaire et l’utilisabilité de ce dernier. Pourtant, les méthodes traditionnelles de gestion des qualifications sont souvent lourdes, sources d’erreurs et difficiles à auditer. Et si la digitalisation devenait votre meilleur allié pour transformer ces processus en un levier de performance ?

La qualification des équipements, un enjeu réglementaire
La qualification des équipements est une exigence réglementaire essentielle pour les fabricants de produits de santé à usage humain et vétérinaire. Elle est encadrée par des directives strictes, notamment l’annexe 15 des BPF (Bonnes Pratiques de Fabrication), elle-même issue des GMP (Good Manufacturing Practices).
En effet, on peut mentionner l’organisation réglementaire ci-dessous :
- La Commission européenne édite les GMP : un ensemble de directives obligatoires pour garantir la sécurité, la qualité et l’efficacité des produits de santé, applicable à l’Union Européen.
- Ces règles sont ensuite surveillées par des organismes nationaux. En France : l’ANSM (Agence Nationale de Sécurité du Médicament) est chargée de la traduction des GMP en BPF et de leur application.
- Aussi, à l’échelle mondiale : la FDA (Food and Drug Administration) est l’autorité compétente pour le marché américain.
Cela est également complété par les normes : on peut ainsi citer des textes de référence liés à la validation des équipements tels que l’ISO 9001 (Système de gestion de la qualité) ou l’ISO 13485 (dispositifs médicaux), etc.
Comprendre la qualification des équipements et ses étapes
Dans les environnements fortement réglementés, les équipements doivent être qualifiés en suivant les phases optionnelles et obligatoires suivantes :
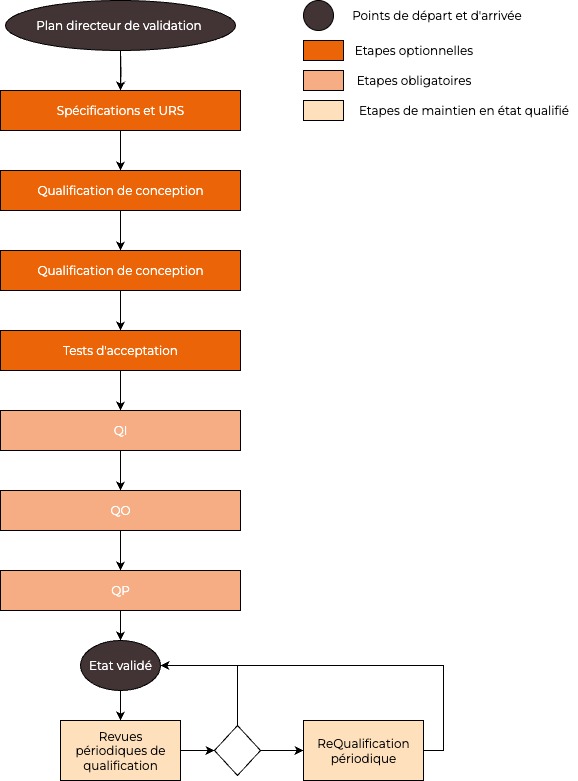
- Plan de validation : Définit le programme, la planification, les objectifs, le périmètre et l’organisation de la qualification.
- Spécifications et URS : Analyse fonctionnelle des besoins sous forme d’URS, cette étape est mise en œuvre en fonction du niveau de complexité et de criticité de l’équipement.
- Qualification de conception : Vérification de la conformité au cahier des charges, aux URS et à la réglementation en vigueur. Cette étape est mise en œuvre en fonction du niveau de complexité et de criticité de l’équipement.
- Test d’acceptation : Vérification sur site fournisseur et à réception de l’équipement. Cette étape est mise en œuvre en fonction du niveau de complexité et de criticité de l’équipement.
- QI – Qualification d’Installation : Cette étape s’assure de la qualité de la livraison, de l’installation et de la configuration des équipements.
- QO – Qualification Opérationnelle : Elle valide que les équipements et leurs composants fonctionnent correctement dans la plage de fonctionnement cible.
- QP – Qualification de Performance : Cette dernière phase évalue la fiabilité et la capacité de fonctionnement dans une utilisation réelle de l’équipement.
- Etat validé : Consiste au statut de conformité et à la documentation complète des différentes phases précédentes.
- Revues périodiques de qualification : Réalisé à fréquence pour contrôler les équipements et la nécessité d’une requalification complète ou partielle éventuelle.
- ReQualifications périodiques : Vise à vérifier que l’équipement fonctionne toujours et fonctionnera toujours de manière fiable et sécurisée d’ici la prochaine requalification.
Pourquoi la digitalisation des qualifications est-elle essentielle ?
- L’intégrité des données (data integrity) et la capacité de la démontrer,
- La traçabilité (audit trail) via des enregistrements centralisés et horodatés.
- La signature électronique sécurisée.
- La centralisation des données et de la documentation dans un outil unique,
- La facilité de mise à jour et versionnage,
- La facilité d’accès, de recherche et de partage des informations,
- La capacité d’exploitation des données,
- La fiabilité et la rapidité des processus grâce aux alertes et tableaux de bords.
- Facilite le bon déroulement des inspections/audits,
- Améliore la collaboration et le travail d’équipe,
- Renforce la capacité à démontrer la conformité,
- Optimise les temps et les coûts liés aux qualifications,
- Le Titre 21 CFR Partie 11 est une section du Code des Réglementations Fédérales des États-Unis. Elle établit les exigences de la Food and Drug Administration (FDA) concernant les enregistrements électroniques et les signatures électroniques.
Trois approches possibles pour la gestion des qualifications
Gestion via répertoire partagé et tableurs Excel : un fonctionnement risqué
Certaines entreprises continuent d’utiliser une gestion 100 % papier ou des tableurs Excel. Si cette approche présente un faible coût initial, elle devient rapidement une source de complications :
- Difficulté à retrouver les documents en cas d’audit ou d’inspection,
- Erreurs humaines fréquentes et manque de standardisation,
- Processus longs, ralentissant les cycles de qualification.
- Réalisation réactive basée sur des responsables qualifications méticuleux,
Cette solution peut convenir à de petites structures, mais son respect des exigences réglementaires dépend fortement du niveau de rigueur mis en place autour de son utilisation.
Digitalisation partielle via GED : un compromis avec des limites
Certaines entreprises choisissent une approche intermédiaire, où seuls certains aspects du processus de qualification sont digitalisés au travers d’une GED :
- Capitalisation des documents au sein d’un espace centralisé,
- Utilisation d’un logiciel sécurisé et collaboratif,
- Validation via signature électronique des documents,
- Recherche simple de documents.
Ce modèle permet une transition progressive, mais pose encore des problèmes :
- Une traçabilité encore imparfaite, les données issues des protocoles ne sont pas tracées en modification, seul le document l’est.
- Impossibilité de visualiser l’historique des qualifications successives d’un équipement,
- Un manque d’alertes liées à la planification des (re)qualifications approchantes,
- Un manque d’interopérabilité avec les autres données du cycle de vie de l’équipement (pannes, maintenances préventives, etc.),
Cette approche peut être un bon premier pas vers la digitalisation, mais n’apporte pas tous les bénéfices escomptés d’un logiciel dédié.
Digitalisation complète : une gestion optimisée et performante
Adopter un outil spécialisé pour la gestion des qualifications permet de transformer un processus contraignant en un levier de performance. Une solution comme TEEXMA offre :
- Une vue documentaire et équipement, offrant des points de vues complémentaires,
- La complète digitalisation des protocoles qui permet une traçabilité totale sur chaque donnée,
- Une gestion centralisée et proactive des (re)qualifications à réaliser,
- La gestion de workflows de validation multi-profils, accélérant ces circuits,
- La génération de documents sécurisés basés sur les données capitalisées,
- La GED intégrée avec gestion des visionnages, diffusion, etc.
- Une signature électronique et un audit trail conforme avec la 21 CFR Part 11,
- Une gestion simplifiée des audits, avec des recherches et historiques accessibles en un clic.
- Un calcul automatique des prochaines échéances et alertes associées.
Bien que nécessitant un investissement initial plus important, cette approche garantit une conformité réglementaire optimale et une réactivité inégalée.
En résumé, la digitalisation des qualifications est une évolution incontournable :
- Si la gestion manuelle peut sembler économique, elle devient rapidement un frein au développement et à la conformité réglementaire.
- Une digitalisation partielle via GED peut être une transition intéressante, bien qu’elle ne résolve pas toutes les problématiques afférentes aux secteurs réglementées.
- Opter pour une solution dédiée et métier est le choix le plus optimal tant d’un point vu réglementaire, qu’organisationnel.
BASSETTI : l'expertise au service de la conformité réglementaire
Pour accompagner les entreprises dans cette transformation digitale, BASSETTI propose son logiciel TEEXMA, une solution conçue pour répondre aux besoins des secteurs réglementés et permettant de répondre aux approches 2 (GED) et 3 (logiciel dédié) présentées ci-avant.
Avec TEEXMA for Maintenance, vous assurez la compatibilité réglementaire afférente aux qualifications des équipements, et vous pouvez mutualiser votre application logicielle avec les autres services qui le souhaitent : maintenance (offre GMAO), métrologie (offre métrologie), Qualité (Offre SMQ), laboratoire (offre LIMS), production (offre MES).